Current Biology | 巨噬细胞通过细胞因子扩增加速肿瘤生长
发布时间:2025-09-08
浏览次数:15363
作者:东极药物
通过对巨噬免疫细胞在肿瘤中遭遇濒死癌细胞过程的研究,名古屋大学科学家发现了一种加速肿瘤生长的机制。当肿瘤内部癌细胞开始死亡时,其表面会暴露出濒死信号。巨噬细胞随后检测到这些信号,并对濒死癌细胞进行吞噬···
通过对巨噬免疫细胞在肿瘤中遭遇濒死癌细胞过程的研究,名古屋大学科学家发现了一种加速肿瘤生长的机制。
当肿瘤内部癌细胞开始死亡时,其表面会暴露出濒死信号。巨噬细胞随后检测到这些信号,并对濒死癌细胞进行吞噬。研究者以果蝇为模型发现,该过程会触发特定细胞因子的产生,这些因子能激活残存癌细胞的生长信号。
这些细胞(巨噬细胞)随后会产生更多的细胞因子,引发一种意外的连锁反应,反而促进了肿瘤的生长。由名古屋大学生物科学系的Shizue Ohsawa教授(博士)领导的研究团队表明,通过阻止巨噬细胞吞噬垂死的癌细胞或阻断细胞因子的产生来阻断这一通路,能显著抑制肿瘤生长。
Ohsawa教授指出,靶向巨噬细胞与垂死癌细胞之间的这种相互作用可能成为治疗人类癌症的新方法:“由于果蝇和人类之间的分子通路在进化上是保守的,理解这些机制可以解释为何一些癌细胞死亡率很高的癌症仍能快速生长,并有望推动更有效的治疗方案。”
资深作者Ohsawa与第一作者、名古屋大学大学院理学研究科博士生Eri Hirooka及其同事在《Current Biology》杂志上发表了一项研究,论文题为“Macrophages promote tumor growth by phagocytosis-mediated cytokine amplification in Drosophila”。该团队在论文中总结道:“我们的研究揭示了一种新的非自主肿瘤进展机制,即垂死的致癌细胞激活了巨噬细胞的吞噬功能,而这一功能传统上被视为一种肿瘤抑制机制。”

作者们指出,肿瘤微环境中癌细胞与基质细胞(包括炎症细胞、免疫细胞和成纤维细胞)之间复杂的相互作用,越来越被认为是肿瘤进展的关键驱动因素。在这些基质细胞中,肿瘤相关巨噬细胞(TAMs)代表了主要的吞噬性免疫细胞群。该团队写道:“它们的存在与大多数实体瘤类型的肿瘤发生、治疗反应有限以及不良预后相关,然而其中的因果机制仍不明确。”
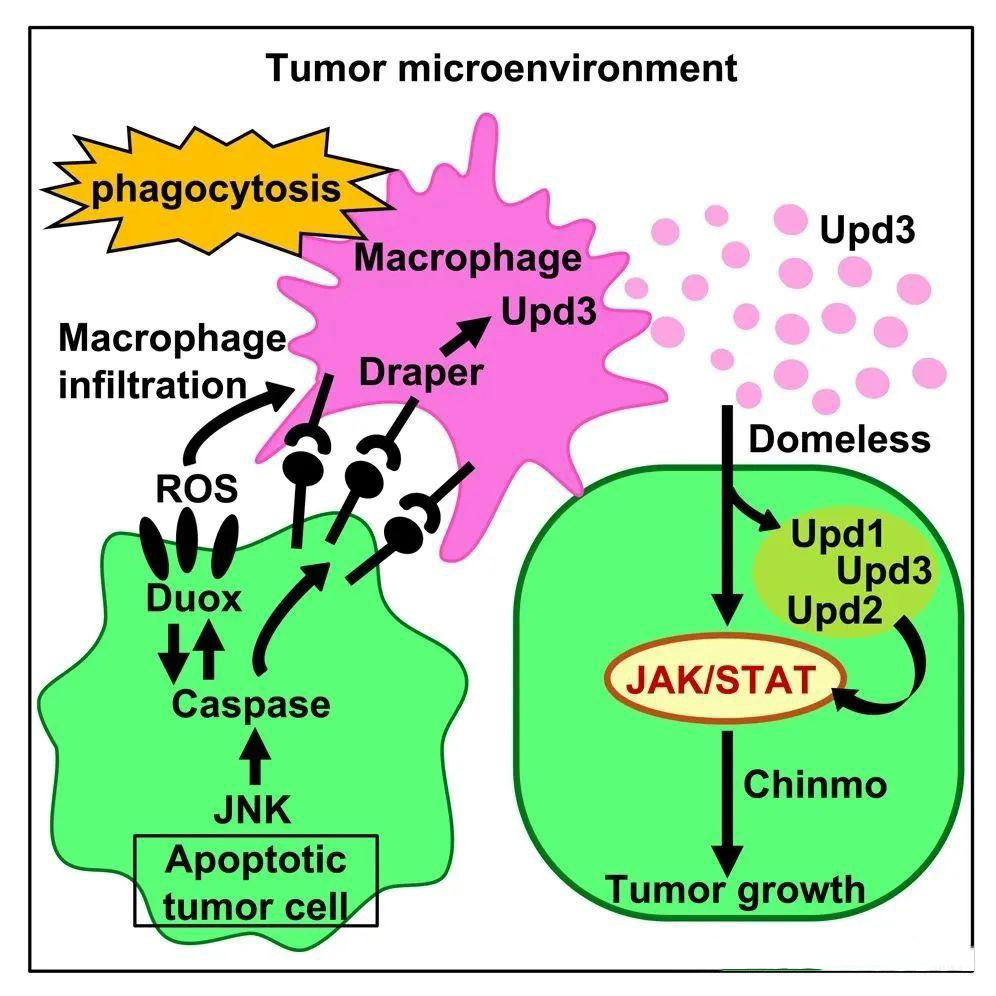
图文摘要
果蝇(Drosophila)的细胞免疫系统主要包括血细胞(hemocytes),其中数量最多的亚型是浆血细胞(plasmatocytes)。作者们将其描述为专业的吞噬细胞,类似于脊椎动物的巨噬细胞,它们“吞噬微生物、细胞碎片和异物,并通过分泌炎性细胞因子来启动体液免疫反应”。该团队指出,与哺乳动物的TAMs相似,已有研究表明果蝇的血细胞也能促进肿瘤组织生长。“然而,致癌细胞如何导致血细胞发挥非自主性影响(non-autonomous influences)从而驱动肿瘤生长的机制,在很大程度上仍难以捉摸。”
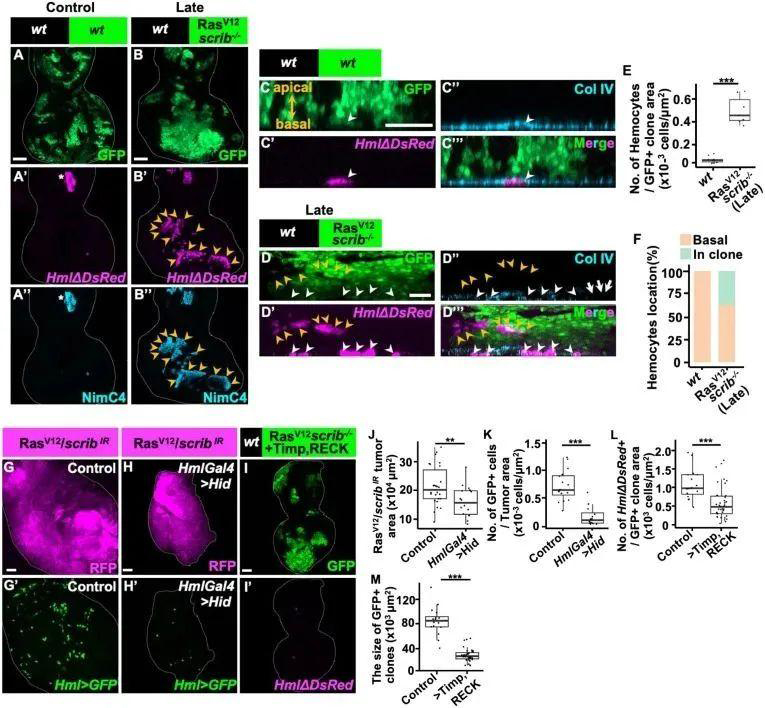
成熟的浆细胞样吞噬细胞促进RasV12/scrib肿瘤的生长
该团队在报告中提到,他们转向使用了转基因果蝇进行研究。Hirooka说:“我们使用转基因果蝇来研究癌症,因为它们的免疫系统与我们相似,并且在实验室研究中提供了一个强大的模型系统。我们在它们的眼组织中制造了微小的肿瘤,并使用荧光标记物在显微镜下实时追踪癌细胞和巨噬细胞。”
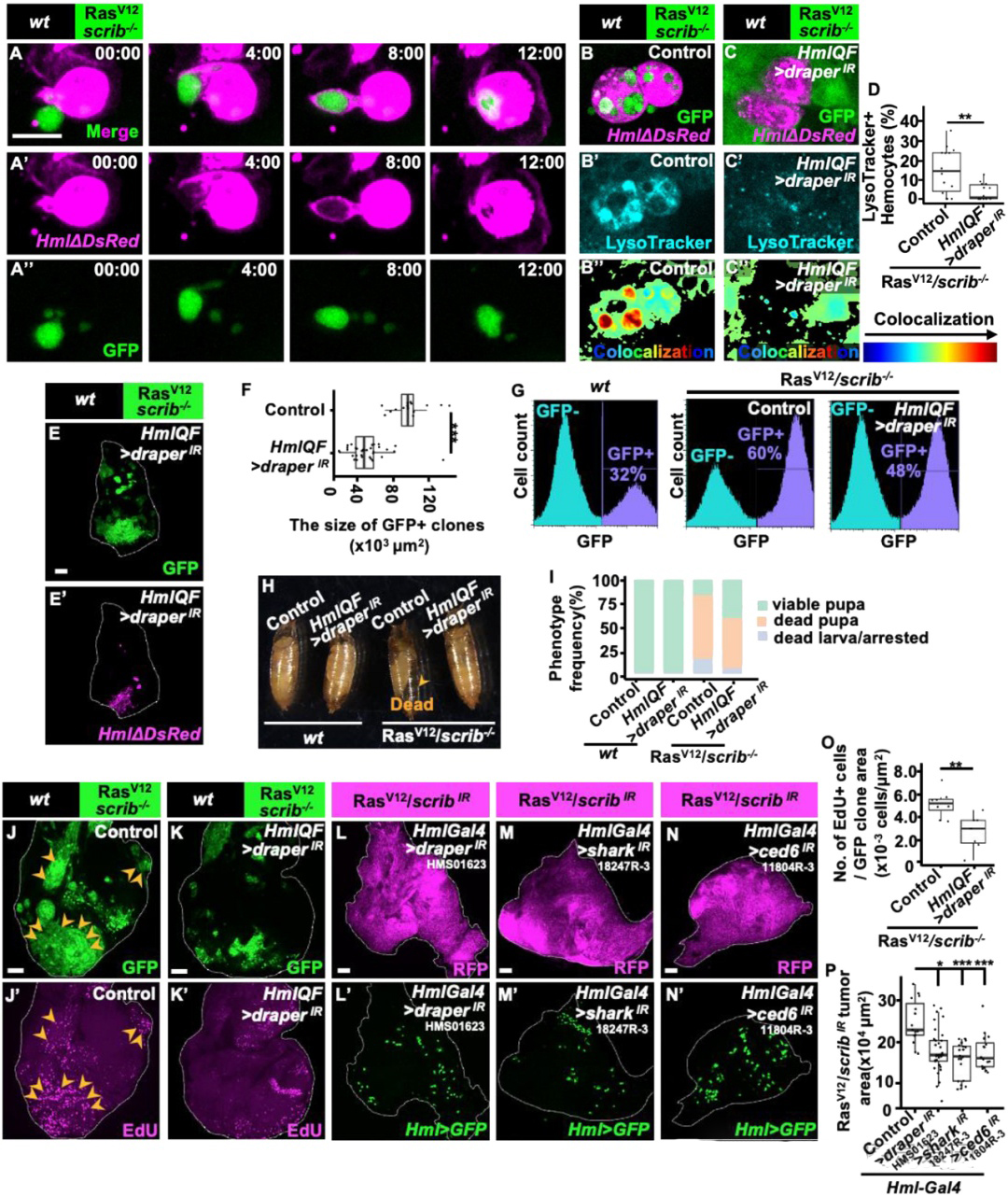
成熟吞噬性浆细胞中的Draper通路促进RasV12/scrib肿瘤生长
为了解这些细胞如何相互作用,研究人员打开和关闭了特定基因,添加或去除了特定蛋白质,并测量了这些操作对肿瘤生长的影响。他们观察到巨噬细胞吞噬垂死的癌细胞,并测量了在此过程中产生的细胞因子信号。
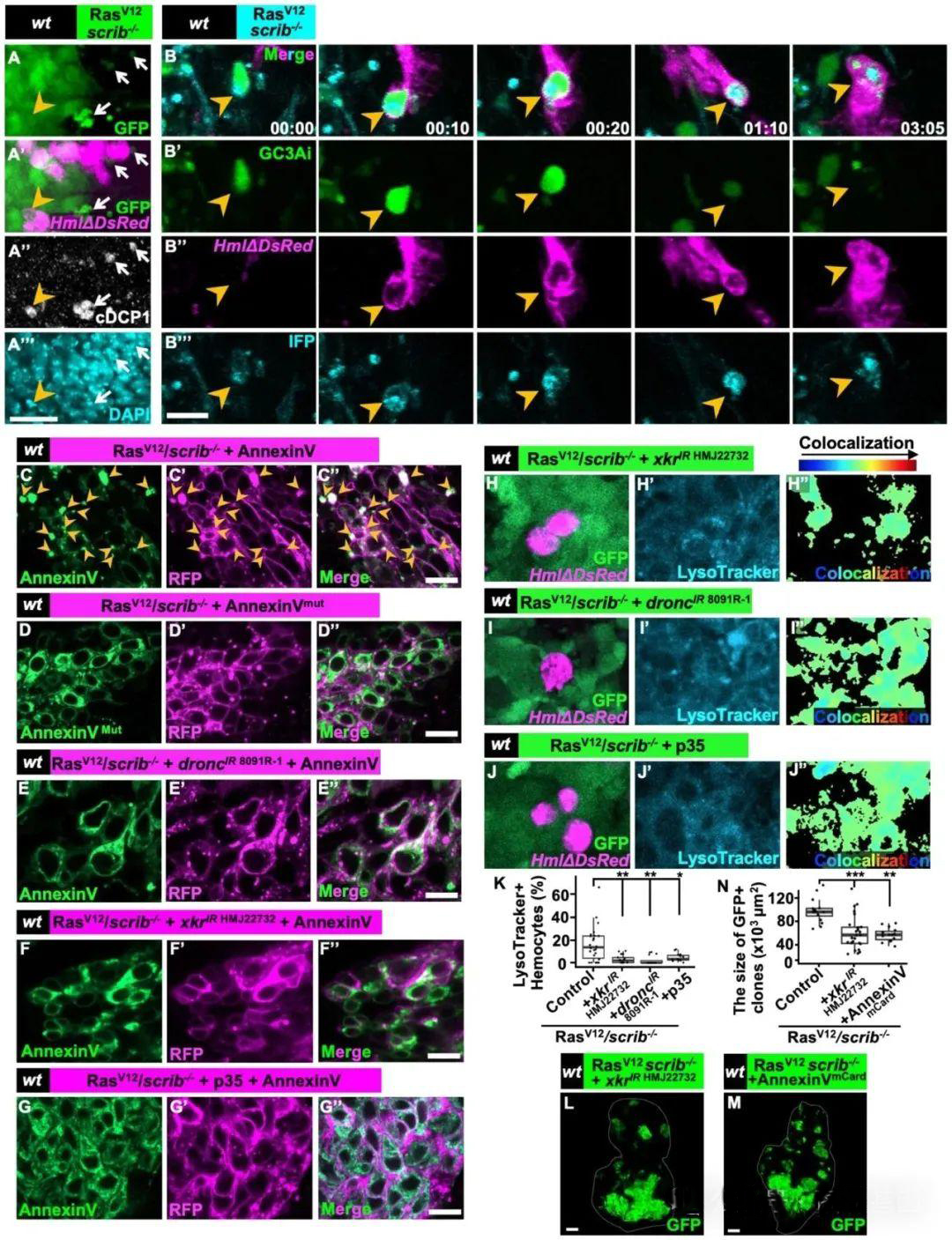
在RasV12/scrib突变细胞中,caspase依赖的磷脂酰丝氨酸(PS)暴露是成熟浆细胞进行吞噬作用所必需的
他们发现并描述了成熟的吞噬性浆血细胞(mature phagocytic plasmatocytes)与致癌性的RasV12/scrib细胞(一种成熟的果蝇恶性肿瘤模型)之间存在的“意料之外的细胞间相互作用”。他们的研究表明,当果蝇体内的巨噬细胞吞噬垂死的癌细胞时,它们会产生一种名为Upd3炎性细胞因子,这种蛋白质与人类的IL-6(白细胞介素-6)类似。这种Upd3会激活存活癌细胞内部的JAK和STAT蛋白。
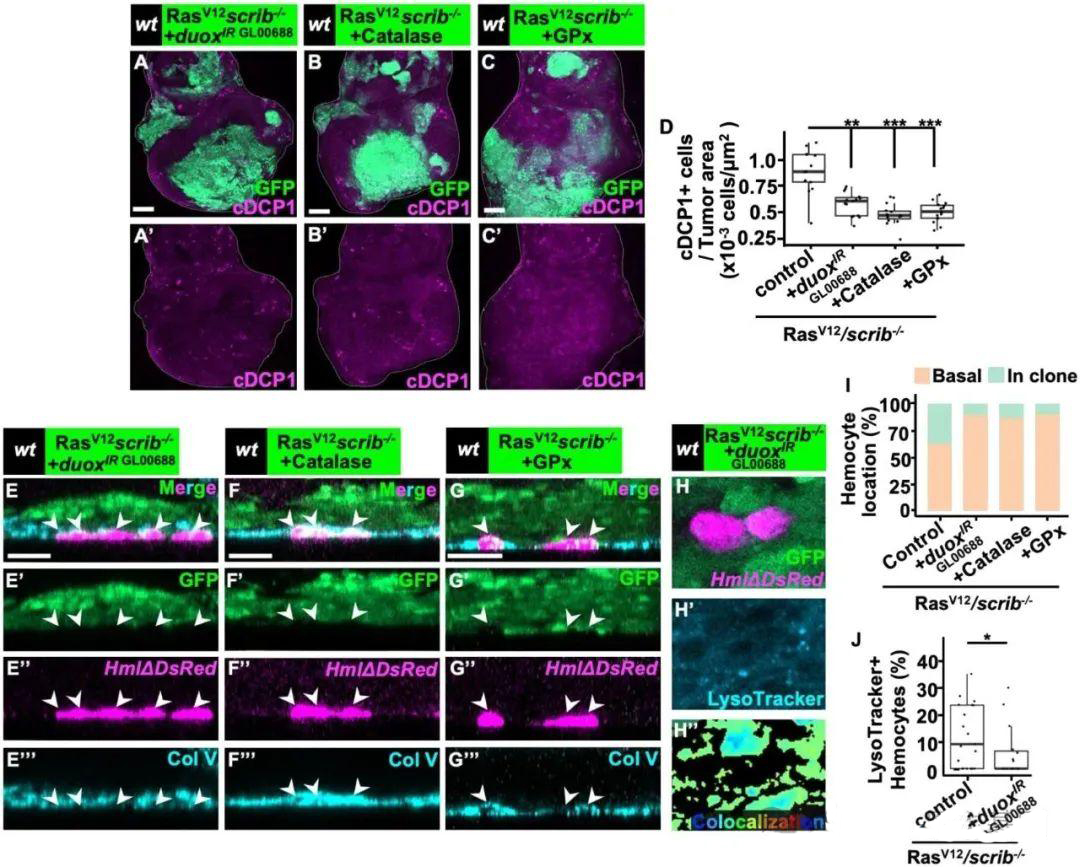
Caspase-ROS相互作用调控成熟吞噬浆细胞的浸润及RasV12/scrib肿瘤的生长
这些蛋白通常协调免疫反应和组织修复,但癌细胞劫持了这一过程:它们开启相关基因,使其自身也产生Upd3,从而增强了JAK和STAT的激活,并促进了肿瘤的生长。他们写道:“我们观察到,成熟的浆血细胞在这些肿瘤内部吞噬了胱天蛋白酶(caspase)激活的RasV12/scrib细胞。值得注意的是,正是通过这种吞噬性相互作用,成熟的浆血细胞分泌了炎性细胞因子Upd3,从而诱导了RasV12/scrib肿瘤中upd基因的表达和JAK/STAT信号通路的激活,最终促进了肿瘤的生长。”
研究人员随后发现,当他们通过基因手段降低巨噬细胞吞噬垂死癌细胞的能力,或降低Upd3的产生时,肿瘤生长显著减缓。这些结果挑战了“增强免疫细胞吞噬能力在癌症治疗中总是有益”的假设——许多疗法旨在增强免疫细胞活性,但这项研究表明这可能会适得其反。
结果表明癌细胞比预想的更狡猾。它们不仅从免疫细胞接收生长信号,还通过自身产生Upd3来主动增强这些信号。研究团队指出,这些发现表明,RasV12/scrib 肿瘤“劫持”(co-opt)了这种通常在感染、组织修复和再生过程中被激活的保守细胞因子放大机制,以加速自身生长。“这种对免疫调节机制的‘劫持’(hijacking)可能是肿瘤进展的关键策略,由复杂的器官间通讯所驱动。”
该机制可能普遍存在于不同物种中,因为启动整个过程的濒死癌细胞在肿瘤中普遍存在,在晚期癌症中尤为常见。
文章出自:验外实包 想了解更多请关注:http://www.dj-cro.com/